Jetzt kaufen



Wunden heilen besser, wenn sie feucht behandelt werden [29]. Die HydroTherapy mit HydroClean und HydroTac ist dazu eine passende Therapieoption. Die Behandlung ist zumeist aber auch ein langwieriger Prozess, der die Compliance des Patienten erfordert. Und um diese zu stärken, sollte der Patient über Wundheilungsprozesse und Wirkungsweise der HydroTherapy gut informiert sein.
Es begann mit den Arbeiten von George D. Winter, die 1962 im Wissenschaftsmagazin „Nature“ erstmals veröffentlicht wurden. Winter wies nach, dass ein feuchter und permeabler (durchlässiger) Wundverband und das damit erzielte „moist wound healing“ zu einer schnelleren Wundheilung führt als ein trockenes, der Luft ausgesetztes Wundmilieu [29].
Diese Erkenntnis, die im Verlauf der folgenden Jahrzehnte zur Methode der Feuchttherapie führte, darf mit Recht als Meilenstein im Wundmanagement betrachtet werden: Das feuchte Milieu fördert die Wundreinigung, schont heilungsfördernde Substanzen und Zellen auf der Ulkusfläche, begünstigt Wachstum und Vermehrung von Fibroblasten und Epithelzellen und wirkt stark analgetisch [1].
In den Anfängen der Feuchttherapie wurde zum Feuchthalten der Verbände physiologische Kochsalzlösung (NaCl 0,9 %) verwendet. Da sich diese aber in Laborversuchen (in vitro) als nicht ganz physiologisch für Fibroblasten und Epithelzellen [1] erwies, wurde isotone Ringer-Lösung eingesetzt. Sie enthält neben Natriumchlorid auch Kalium- und Calciumchlorid, sodass sie ein gutes Nährmedium für lebende Zellen bzw. Frischgewebe darstellt.
Für den feuchten Wundverband wurde eine dünne Mullkompresse mit Ringer-Lösung befeuchtet und die Wundfläche damit abgedeckt. Um die Mullkompresse permanent feucht zu halten, musste die Kompresse etwa alle zwei bis vier Stunden nachbefeuchtet werden, um ein Austrocknen und Verkleben zu verhindern. Dies war zeit- und personalaufwendig, damit auch kostenintensiv und in der häuslichen Wundversorgung gar nicht durchführbar.
Mit der Entwicklung der HydroTherapy mit HydroClean und HydroTac konnte HARTMANN diese Probleme alle auf einmal lösen. Nunmehr kann die feuchte Wundbehandlung in allen Bereichen der Medizin und Pflege – stationär und ambulant – problemlos durchgeführt werden.
Obwohl die Feuchttherapie mittlerweile als Standard in der Behandlung chronischer Wunden gilt, da sie nachweislich die Wundversorgung verbessert, ist sie beim Patienten noch nicht in dem Ausmaß angekommen, das Wundexperten gerne sehen würden. Viel zu oft werden Wunden zum Nachteil der Patienten noch „trocken“ behandelt. Zudem werden Patienten und Angehörige auch eher selten über die Vorteile einer feuchten Wundbehandlung informiert.
Das innovative Konzept der HydroTherapy, die Wirkungsweise und Handhabung sind einfach zu erklären. Informationen dazu finden sich in diesem Beitrag. Sind Patient und Angehörige aber erst einmal „aufgeklärt“ und erleben sie mit der HydroTherapy eine Wundbehandlung, die ihnen ein Stück Lebensqualität zurückgibt, wird dies auch zu einer verbesserten Compliance führen, die bei den oft langen Behandlungszeiten bei chronischen Wunden erforderlich ist.
Wie sollte eine effektive Wundheilung aussehen? Wie lässt sich die Bakterienlast in Wunden reduzieren? Werden wirkstoffhaltige Wundauflagen für ein zeitgemäßes Wundmanagement benötigt? Diese und andere Themen diskutierten Experten aus Medizin, Wundmanagement und Pflege im August 2018 in Frankfurt. Sehen Sie hier Ihre Antworten.
Wir verwenden zur Einbindung unserer YouTube-Videos den sog. erweiterten Datenschutzmodus. Hierbei wird das Setzen von YouTube-Cookies auf Ihrem Gerät zunächst blockiert, wenn Sie unsere Website besuchen. Erst beim Anklicken des Vorschaubildes wird das Video geladen. Dies wird dadurch ermöglicht, dass Sie technisch auf die YouTube-Website weitergeleitet werden. Ab diesem Zeitpunkt haben wir aber keine Kontrolle mehr darüber, welche Daten an YouTube gesendet werden und welche Cookies oder andere Mittel zum Nutzer-Tracking oder zur Analyse des Nutzerverhaltens von YouTube einsetzt werden. Nähere Informationen zur Cookie-Verwendung durch YouTube finden Sie in der Datenschutzerklärung von Google und der Cookie-Policy von Google. Das einmal gesetzte YouTube-Cookie können Sie jederzeit in Ihrem Browser löschen. Weitere Informationen zur Löschung von Cookies finden Sie unter anderem auf der Webseite Ihres Browser-Anbieters.
Unsere Haut besitzt die wunderbare Fähigkeit, sich im Falle einer Verletzung selbst heilen zu können. Ist nur die oberste Hautschicht verletzt, kann sie sich sogar narbenlos regenerieren und die neue Hautschicht unterscheidet sich in keiner Weise von der vorhergehenden. Sind jedoch tiefere Hautschichten geschädigt, muss Ersatzgewebe aufgebaut werden, um den Hautdefekt zu schließen. Das Ersatzgewebe bildet sich dann zur sichtbaren Narbe um.
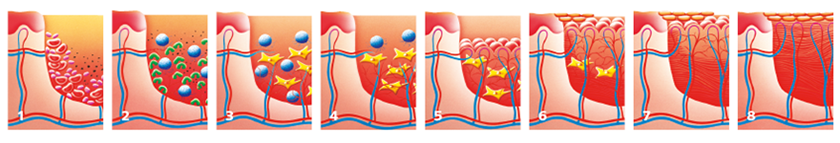
Die normale Heilung tiefer Hautwunden läuft dabei in immer der gleichen Weise in bestimmten Phasen ab: Unmittelbar nach der Verletzung erfolgt die Blutstillung. Dann werden in der sog. Reinigungsphase geschädigtes Gewebe und Bakterien durch körpereigene Blut- und Abwehrzellen eliminiert. Ist die Wunde sauber, kann durch Bindegewebszellen Ersatzgewebe, das sog. Granulationsgewebe aufgebaut werden. Deshalb wird diese Wundheilungsphase kurz als Granulationsphase bezeichnet. Die abschließende Überhäutung der Wunde durch Epithelzellen – Zellen der obersten Hautschicht – findet in der sog. Epithelisierungsphase statt.
Im Falle chronischer Wunden ist die Heilung allerdings viel schwieriger. Denn chronische Wunden sind in den überwiegenden Fällen Gewebezerstörungen, die sich von inneren Hautschichten nach außen hin entwickeln. „Ein Geschwür bricht auf“ wie es umgangssprachlich heißt, ist somit eine korrekte und verständliche Beschreibung dieses Vorgangs. Ursache für die Gewebezerstörung sind zumeist Durchblutungsstörungen des betroffenen Hautgebietes, beispielsweise durch Gefäßerkrankungen, Diabetes mellitus oder Druckeinwirkungen auf die Haut (Dekubitus).
Die Durchblutungsstörungen führen im Verlauf der Erkrankung zu immer stärkerem Nährstoff- und Sauerstoffmangel, bis schließlich Gewebezellen absterben. Es bilden sich Nekrosen, das sind abgestorbene Gewebeareale, die durch ihre schwarze und ledrige Beschaffenheit auffallen. Eine normale Wundheilung ist dann unter diesen Bedingungen nicht mehr möglich. Die körpereigene Zellabwehr ist auch nicht mehr in der Lage, die Wunde aus eigener Kraft zu reinigen. Hilfe von außen ist dringend notwendig: Durch eine gründliche Wundreinigung müssen schnellstmöglich alle wundheilungsstörenden Faktoren wie Nekrosen, Beläge und Keime aus der Wunde entfernt werden. Dazu hat sich die feuchte Wundbehandlung bewährt.
Austrocknung ist der Feind aller lebenden Zellen. Dies gilt erst recht für geschädigtes und offen liegendes Wundgewebe. Es muss durch feuchte Verbände geschützt und bei der Heilung unterstützt werden. Feuchthalten der Wunde

Unter den hydroaktiven Wundauflagen nimmt HydroClean eine Sonderstellung ein, denn es entfaltet in der Wunde eine aktive Saug-Spülwirkung (siehe Grafik).
Basis für den einzigartigen Saug-Spül-Mechanismus ist der Saugkern aus wirkstofffreiem Superabsorber (SAP), der mit Ringerlösung getränkt ist. Diese wird kontinuierlich an die Wunde abgegeben. Durch die permanente Zufuhr von Ringerlösung werden Nekrosen und Beläge aktiv aufgeweicht, abgelöst und „ausgespült“, was die schnelle und effektive Reinigungswirkung [4] von HydroClean erklärt. Gleichzeitig wird das mit Keimen belastete Wundexsudat in den Superabsorber-Kern aufgenommen und dort sicher gebunden [2-5,10-14]. Dieser Austausch funktioniert, weil der Superabsorber eine größere Vorliebe für das proteinhaltige Wundexsudat als für die salzhaltige Ringerlösung besitzt. Sobald dann Beläge, Nekrosen und Bakterien entfernt sind, kann der Aufbau von Granulationsgewebe beginnen.
Untersuchungen [7] haben auch ergeben, dass HydroClean bestimmte Enzyme (Matrix-Metalloproteasen [MMPs]) reduziert. MMPs stören die Heilungsprozesse, wenn sie im Überfluss vorhanden sind, was vor allem bei chronischen Wunden der Fall ist. Gemeinsam mit dem Wundexsudat werden die MMPs in den Saug-Spülkern aus SAP aufgenommen, dort sicher gespeichert und damit inaktiviert. Das Wundmilieu kann sich normalisieren.
Insgesamt steht mit HydroClean eine hydroaktive Wundauflage zur Verfügung, die die Wundreinigung fördert [2,4,11,15-19], entweder als alleinige Maßnahme oder in Fortführung anderer Débridementmethoden. Nekrosen lösen sich häufig bereits in den ersten Tagen der Behandlung [4] oder weichen so stark auf, dass sie mechanisch entfernt werden können. Nachgewiesen wurde auch eine erhebliche Reduktion der Bakterienlast [2,3,23]. Zudem berichten Patienten über weniger Schmerzen unter der HydroClean-Behandlung [3,4,10,12,16,18-22].
Mit der Reepithelisierung und der damit verbundenen Wiederherstellung der schützenden Hautbarriere kommt die Wundheilung zum Abschluss. Dieser Prozess kann durch den innovativen Schaumverband HydroTac mit AquaClear Gel Technologie aktiv beeinflusst und beschleunigt werden [5,6,9].
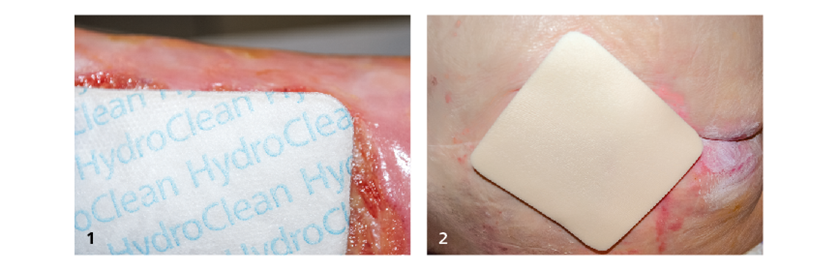
Ist die Wunde im Rahmen der HydroTherapy im ersten Schritt mit HydroClean gereinigt und konditioniert, kommt im zweiten Schritt der Schaumverband HydroTac mit AquaClear Gel Technologie zur Anwendung.
Basis der AquaClear Gel Technologie sind sog. hydratisierte Polyurethane, die zwei Funktionen haben: Sie absorbieren Flüssigkeit, geben aber auch je nach Bedarf der Umgebung Feuchtigkeit ab. Damit sorgt HydroTac für eine optimale Feuchtigkeitsregulierung, was die Bildung von Granulations- und Epithelgewebe fördert [3,10,18,25-28].
Die hydratisierten Polyurethane können aber noch mehr: Entsprechend eines bestimmten Effektes, der als „molecular crowding“ beschrieben ist, steigern sie die Konzentration von Wachstumsfaktoren und erhöhen die Aktivität von Epithelzellen, um den Heilungsprozess zu stimulieren. Die AquaClear Gel Technologie sorgt so für eine 3-mal höhere Konzentration an Wachstumsfaktoren [5,6,24] und damit für eine schnellere Wundheilung.
Literatur
[1] W.O. Seiler; HARTMANN WundForum 2/2007, Feuchttherapie chronischer Hautulzera mit Ringer’scher Lösung: physiologisch, heilungsfördernd, schmerzlindernd.
[2] Atkin, L. and Ousey, K. (2016). Wound bed preparation: A novel approach using HydroTherapy. British Journal of Community Nursing 21 (Supplt. 12), pp. S23-S28.
[3] Ousey, K. et al. (2016). HydroTherapy Made Easy. Wounds UK 12(4).
[4] Humbert, P. et al. (2014). Protease-modulating polyacrylate-based hydrogel stimulates wound bed preparation in venous leg ulcers – a randomized controlled trial. Journal of the European Academy of Dermatology and Venereology 28(12), Seiten 1742-1750.
[5] Smola, H. (2016). Simplified treatment options require high-performance dressings – from molecular mechanisms to intelligent dressing choices. EWMA 2016. Bremen, 11.-13. Mai 2016.
[6] Smola, H. et al. (2016). Hydrated polyurethane polymers to increase growth factor bioavailability in wound healing. HydroTherapy Symposium: A New Perspective on Wound Cleansing, Debridement and Healing. London, 3.März 2016.
[7] Eming, S., Smola, H., Hartmann, B. et al. (2008). The inhibition of matrix metalloproteinase activity in chronic wounds by a polyacrylate superabsorber. Biomaterials 29: 2, 2932-2940
[8] ISBN Monograph. 978-1-944788-63-6-ISBN Services
[9] Kaspar, D. (2011). Therapeutic effectiveness, compatibilityand handling in the daily routine of hospitals or physicians’s practices. HARTMANN Archivdaten: Hydro-Responsive Wound Dressing (HRWD) und AquaClear Technologie sind Marken von HARTMANN
[10] Ousey, K. et al. (2016). Hydro-Responsive Wound Dressings simplify T.I.M.E. wound management framework. British Journal of Community Nursing 21 (Supplt. 12), pp. S39-S49.
[11] Spruce, P. et al. (2016). Introducing HydroClean® plus for wound-bed preparation: a case series. Wounds International 7(1), pp. 26-32.
[12] Ousey, K. et al. (2016). HydroClean® plus: a new perspective to wound cleansing and debridement. Wounds UK 12(1), pp. 94-104.
[13] Atkin, L. and Rippon, M. (2016). Autolysis: mechanisms of action in the removal of devitalised tissue. British Journal of Nursing 25(20), Seiten S40-S47.
[14] Kaspar, D. et al. (2015). Economic benefit of a polyacrylate-based hydrogel compared to an amorphous hydrogel in wound bed preparation of venous leg ulcers. Chronic Wound Care Management and Research 2, Seiten 63-70.
[15] Bullough, L. et al. (2016). A multi-centre 15 patient evaluation of a Hydro-Responsive Wound Dressing (HRWD) - HydroClean® plus. HydroTherapy Symposium: A New Perspective on Wound Cleansing, Debridement and Healing. London, 3.März 2016.
[16] Scherer, R. et al. (2015). HydroTherapy®. Anwendungsstudie. Heidenheim: Paul Hartmann AG. (Daten liegen vor.)
[17] Chadwick, P. and Haycocks, S. (2016). The use of Hydro-Responsive Wound Dressing for wound bed preparation in patients with diabetes. Wounds UK Annual Conference. Harrogate, 14.-16. November 2016.
[18] Knowles, D. et al. (2016). HydroTherapy® wound healing of a post amputation site. Wounds UK Annual Conference. Harrogate, 14.-16. November 2016.
[19] Zollinger, C. et al. (2014). HydroTherapy®. Anwendungsstudie. Heidenheim: Paul Hartmann AG. (Daten liegen vor.)
[20] Colegrave, M. et al.(2016). The effect of Ringer’s solution within a dressing to elicit pain relief. Journal of Wound Care 25(4), Seiten 184-190.
[21] O’Brien, D. and Clarke, Z. (2016). The patient experience with a Hydro-Responsive Wound Dressing (HRWD) – HydroClean® plus. HydroTherapy Symposium: A New Perspective on Wound Cleansing, Debridement and Healing. London, 3.März 2016.
[22] Jones, T. and McCracken, K. (2016). HydroClean® plus assists healing of leg ulcers for a patient with systemic lupus erythematosus. Wounds UK Annual Conference. Harrogate, 14.-16. November 2016.
[23] Kaspar, D. et al. (2008). Efficacité clinique du pansement irrigo-absorbant HydroClean® active contenant du polyacrylate superabsorbant dans le traitement des plaies chroniques – étude observationnelle conduite sur 221 patients. Journal des Plaies et Cicatrisations 13(63), Seiten 21-24.
[24] Smola, H. (2015). Stimulation of epithelial migration – novel material based approaches. EWMA-Kongress. London, 13.-15.Mai 2015.
[25] Smola, H. et al. (2014). Hydrated polyurethane polymers to increase growth factor bioavailability in wound healing. EORS-Kongress. Nantes, 2.-4. Juli 2014.
[26] Spruce, P. and Bullough, L. (2016). HydroTac®: case studies of use. HydroTherapy Symposium: A New Perspective on Wound Cleansing, Debridement and Healing. London, 3.März 2016.
[27] Spruce, P. et al. (2016). A case study series evaluation of HydroTac®. HydroTherapy Symposium: A New Perspective on Wound Cleansing, Debridement and Healing. London, 3.März 2016.
[28] Smola, H. et al. (2016). From material science to clinical application – a novel foam dressing for the treatment of granulating wounds. HydroTherapy Symposium: A New Perspective on Wound Cleansing, Debridement and Healing.
[29] George D. Winter. Formation of the scab and the rate of epithelisation of superficial wounds in the skin of the young domestic pig (Nature 193:293 1962)